本品为人血液制品,因原料来自人血,虽然对原料血浆进行了相关病原体的筛查,并在生产工艺中加入了去除和灭活病毒的措施,但理论上仍存在传播某些已知和未知病原体的潜在风险,临床使用时应权衡利弊。
>国内首家血液制品GMP认证企业
>国内首家采用双重病毒灭活工艺用于生产
>国内首家采用全自动采浆机和全自动洗瓶灭菌罐装生产线的生产企业
>血浆优质安全,多道ELISA(酶联免疫法)和核酸扩增技术检测
>不含防腐剂和抗生素,纯度高,稳定性好
>全面与世界接轨的标准化体系认证

请仔细阅读说明书并在医师指导下使用
本品为人血液制品,因原料来自人血,虽然对原料血浆进行了相关病原体的筛查,并在生产工艺中加入了去除和灭活病毒的措施,但理论上仍存在传播某些已知和未知病原体的潜在风险,临床使用时应权衡利弊。
[药品名称]
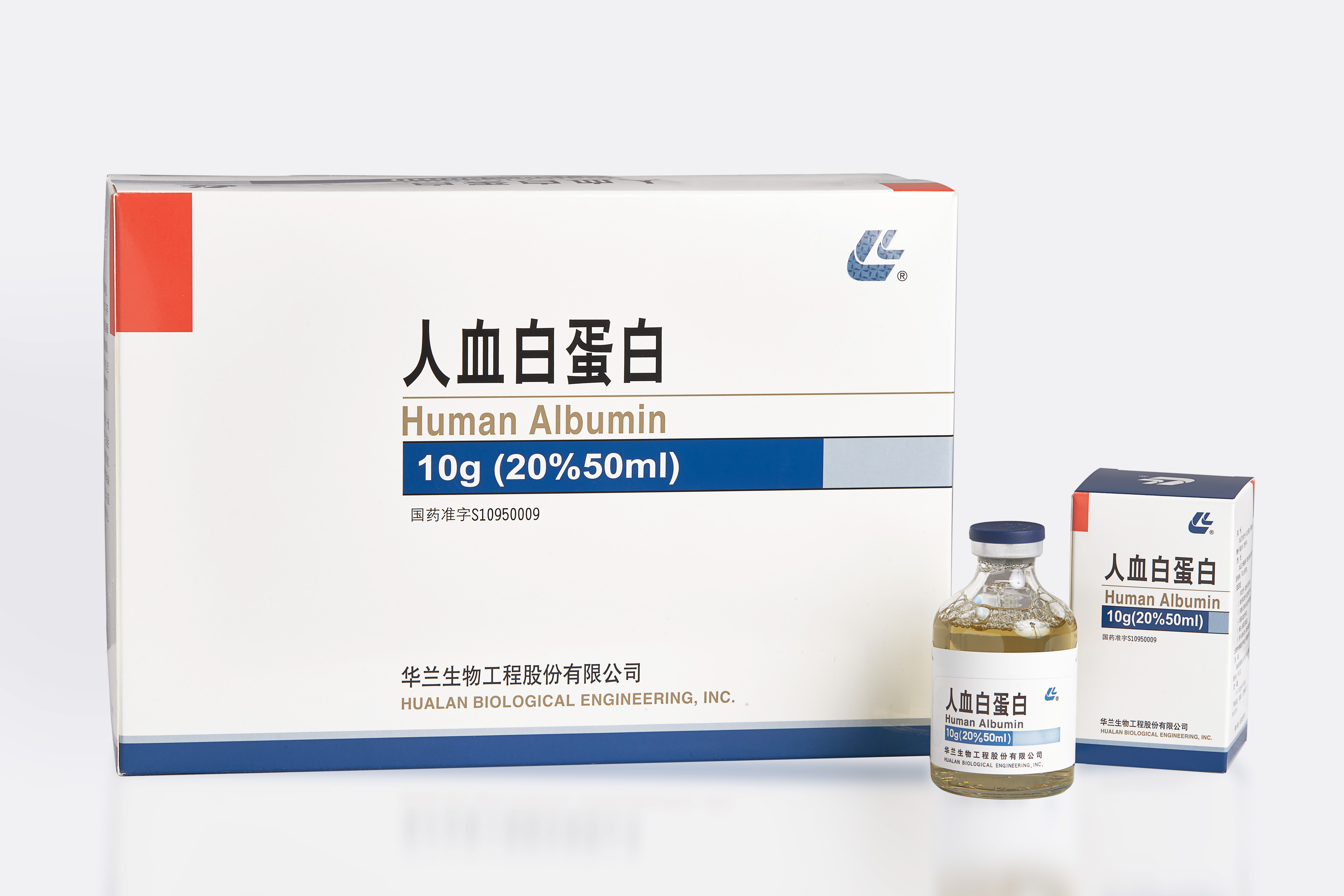
通用名称:人血白蛋白
英文名称:Human Albumin
汉语拼音:Renxue Baidanbai
[成份]
本品活性成份为人血白蛋白,辅料为辛酸钠、氯化钠、注射用水。
[性状]
本品应为略粘稠、黄色或绿色至棕色澄明液体,不应出现浑浊。
[适应症]
1.血容量不足的紧急治疗,遵循相关临床治疗规范。经晶体扩容后仍不能维持有效血容量或伴有低蛋白血症的情况。
2.显著的低白蛋白血症(≤30g/L)的治疗。
3.新生儿高胆红素血症的治疗。
4.急性呼吸窘迫综合征的治疗。
5.用于心肺分流术.特殊类型血液透析、血浆置换的辅助治疗。
[规格]
10g/瓶(20% 50ml)每瓶含蛋白质10g,蛋白质含量为20%,装量50ml。
[用法用量]
本品采用静脉输注。
本品使用时应依据患者的疾病严重程度、有效循环状况和蛋白质损失情况,结合临床治疗需要由医生决定给予的浓度、剂量、输注速率等。通常在开始15分钟内,应缓慢滴注并观察患者反应,之后可根据临床调整输液速度。血容量正常的患者,滴注速率一般不超过2ml/分钟为宜。
| 适应症 | 用法 |
| 血容量不足 | 烧伤患者使用白蛋白的目的应该是将血浆白蛋白浓度保持在25±5 g/L的范围内,血浆渗透压为20mmHg(相当于血浆总蛋白浓度为52g/L)。在烧伤24小时后,根据临床反应调整白蛋白剂量,并开始口服或肠胃外补充氮基酸,不应将长期给予白蛋白作为营养来源。 |
| 低白蛋白血症 | 持续失去白蛋白的严重低白蛋白血症患者可能需要较大的量。一般情况下,低白蛋白血症的治疗目标为血浆白蛋白浓度达30g/L。 |
| 新生儿高胆红素血症 | 在换血治疗之前或期间,可给予白蛋白1g/kg。若为高血容量婴儿患者,建议在换血治疗前约1小时给予。 |
| 急性呼吸窘迫综合征、心肺分流术、特殊类型血液透析、血浆置换的辅助治疗 | 结合患者具体情况及临床应用指南推荐,由医生酌情使用。 |
本品使用注意:
1.呈现混浊、沉淀、异物或瓶子有裂纹瓶盖松动、过期失效等情况不可使用。
2.开启后应立即使用,限一次输注完毕,不得分次或给第二人使用。
3.需使用单独输液通路,使用前用生理盐水冲管。
4.本品可接受的稀释剂包括0.9%氯化钠溶液或5%葡萄糖溶液。禁用灭菌注射用水稀释。若不正确地输入低渗溶液(如灭菌注射用水)稀释人血白蛋白,可能造成严重的溶血反应和急性肾功能衰竭。
[不良反应]
由于人血白蛋白的临床试验数据有限,根据国内外临床应用的报告,静脉注射使用人血白蛋白出现的不良反应按重要程度从高到低列表如下:
| 器官系统 | 不良反应* |
| 免疫系统 | 过敏性休克 超敏反应 |
| 呼吸系统 | 喉头水肿 支气管哮喘 呼吸困难 |
| 循环系统 | 心力衰竭 肺水肿 心肌梗死 心律失常,如房颤、心动过速或心动过缓等 高血压 低血压 |
| 精神障碍 | 精神狂躁不安、亢奋 |
| 消化系统 | 消化道出血 恶心 呕吐 肝功能异常 |
| 泌尿系统 | 溶血反应导致的血尿、少尿、腰痛,严重者可致肾功能受损 |
| 血液系统 | 急性溶血 |
| 神经系统 | 意识丧失 晕厥 头痛 头晕 味觉障碍 |
| 表皮和皮下组织 | 荨麻疹 血管神经性水肿 皮疹 潮红 瘙痒 汗疱疹 |
| 一般反应和注射部位改变 | 发热 寒战 |
(*:以上所列因临床试验数据有限,未能按不良反应发生率进行排序)
[禁忌]
对白蛋白或本品任一成份过敏者。
[警告]
人血白蛋白由人类血液中提取,在生产过程中,已经通过筛查排除既往接触过或体内存在某些病原体感染的血浆供者,并且在制备过程中采取去除或灭活某些病毒的工艺,最大程度降低血液制品传播疾病的风险。但仍不能完全排除人类病原体(包括已知的HBV,HCV,HIV,微小病毒B19等及目前未知或尚未得到鉴定的病原体)潜在感染的可能性。
临床使用人血白蛋白时应权衡利弊,并记录所用产品的生产企业和批号。当发现可能由本品导致的传染性疾病时,应将病例按照相关规定进行报告。
[注意事项]
1.在使用本品的过程中,密切观察生命体征、尿量和电解质等实验室数据,必要时监测血流动力学指标。如果出现超敏反应,则应立刻停止输液。应密切监护患者生命体征,并采取有效的措施,必须警惕发生过敏性休克的风险。如出现休克,应立即开始抗休克的标准治疗。
2.20%,25%人血白蛋白溶液的胶体渗透压相当于血浆渗透压的4~5倍,输注本品时应确保足够的水化。应关注生命体征及实验室指标以免循环超负荷。注意及时补液以免脱水。
3.本品含不高于160mmol/L钠,不高于2mmol/L钾。根据需要监测患者的电解质情况,并采取适当措施恢复或维持电解质平衡。
4.若使用本品代替新鲜血浆进行大剂量血浆置换时,必须监控凝血功能和红细胞压积。须注意确保补充适当的其他血浆蛋白成份,如凝血因子。
5.当大剂量使用本品或快速输注时可能会发生高血容量。在出现心血管容量超负荷的临床症状时,比如头痛、呼吸困难、血压升高、颈静脉充盈、中心静脉压升高、肺水肿,应立即停止输注本品并重新评估患者。
6.对于失代偿性心功能不全、高血压、食管胃底静脉曲张、肺水肿、出血倾向、严重贫血、肾性和肾后性无尿的患者,使用人血白蛋白后可能会带来特定的危险,临床使用本品时需特别注意。
7.对于有病理性毛细血管通透性增加的患者,应结合病因治疗,不宜单独给予本品。
8.对于存在肾功能不全的患者,临床医生根据患者的症状.体征、实验室检查综合评估利弊,酌情使用本品。
9.有临床研究发现,超大剂量使用人血白蛋白相比生理盐水存在增加急性颅脑创伤患者死亡率的风险。但死亡率差异的潜在机理还不明确,建议有严重外伤脑损伤的患者使用本品应遵循相关临床治疗指南。
[孕妇及哺乳期妇女用药]
尚未通过对照临床试验确立本品在人类妊娠期使用的安全性。但是临床经验表明人血白蛋白不会对妊娠过程、胎儿及新生儿产生不良影响。怀孕及哺乳期妇女应仅在必要时由医生权衡并指导使用。
[儿童用药]
除新生儿高胆红素血症外,本品用于儿童患者的适宜剂量应根据临床状态决定。
[老年用药]
尚没有证据显示对成人使用的剂量不适用于老年人。老年患者使用本品时,可参考成人适应症和剂量。特别应评估循环容量和患者的心脏功能情况,而不仅仅是依据血浆白蛋白水平决定用药剂量。
[药物相互作用]
本品需单独使用,不可与溶媒外的其它药物混合。人血白蛋白不得与血管收缩药、蛋白质水解产物或含有乙醇的溶液混合。
[药物过量]
大量使用或快速输注人血白蛋白可能引起脱水、循环负荷增加、充血性心功能衰竭和肺水肿。一旦出现循环超负荷的临床迹象(头痛、呼吸困难和颈静脉充盈),应立刻停止输注。
[药理毒理]
人血白蛋白是人体的正常组分,其最主要的生理功能是维持血液渗透压和转运功能。白蛋白稳定循环血容量,并携带激素、酶、药物、毒素等;静脉给药后在血循环中可被迅速而完全地利用。
[药代动力学]
在正常情况下,人体内的白蛋白总量按体重计算,为4~5g/kg体重,其中血管内占40~45%,55~60%分布在血管外。毛细血管通透性的增高会改变白蛋白的动力学特性,并导致其异常分布,严重烧伤和败血症休克时会发生这种分布异常。
在正常情况下人血白蛋白的平均半衰期是15~20天。白蛋白的合成和代谢的平衡主要靠反馈调节机制实现。最主要的白蛋白代谢依靠细胞内作用,主要由溶酶体蛋白酶完成。
在健康条件下,在输注人血白蛋白2小时内,转运出血管的白蛋白量少于10%。输注白蛋白对血容量的影响有相当大的个体差异。有些患者其血容量可在此后数小时保持上升。但是对于病情严重的患者,部分白蛋白可能漏出于血管外。
[贮藏]
于2~30°C避光保存和运输。
[包装]
硼硅玻璃模制注射剂瓶、溴化丁基橡胶塞包装。1瓶/盒。
[有效期]
自生产之日起36个月。
[执行标准]
《中华人民共和国药典》( 2020年版三部)
[批准文号]
国药准字S10950009
[上市许可持有人]
名称:华兰生物工程股份有限公司
注册地址:河南省新乡市华兰大道甲1号
[生产企业]
企业名称:华兰生物工程股份有限公司
生产地址:河南省新乡市华兰大道甲1号
邮政编码:453003
电话号码:(0373)3519992
传真号码:(0373)3519991
网址:http://www.www.ntkdroof.com